网堵新闻网10月28日电 十大老牌网堵网址药我司钱锋教授课题组近日发现基于胰腺导管癌生物学特征靶向递送NQO1生物激活药物,这将为未来治疗胰腺癌提供潜在创新疗法。
近年来,胰腺癌的发病率呈明显的上升趋势,每年约有1%的上升。据美国癌症协会2022年统计数据显示,胰腺癌患者五年的生存率仅为11%。胰腺癌位居男性恶性肿瘤发病率第10位,女性第8位,占恶性肿瘤相关死亡率的第4位。患者在临床就诊时大部分已为中晚期,患有不可切除的局部晚期或转移性疾病。随着影像、病理、外科手术技术、抗肿瘤药物、药物递送手段等的不断发展,胰腺癌的诊断、治疗迎来了不少机遇与进步。
NAD(P)H:醌氧化还原酶1(NQO1)是一种双电子氧化还原酶,在多种肿瘤中高度富集。NQO1生物激活药物,例如β-lapachone,具有独特的醌结构,被NQO1催化后生成活性氧(ROS)导致未修复的DNA损伤和细胞程序性坏死。然而,由于用药后严重的急性毒性反应,包括溶血性贫血和高铁血红蛋白血症等,使其在不同癌症类型的尝试中以失败告终。此外,β-lap会迅速从血液中清除,并表现出非特异性药物分布,导致肝细胞内出现空泡等组织损伤,使肿瘤部位药物浓度低,治疗效果不佳。本研究旨在探讨如何通过胰腺癌自身的生物学特征,通过递送系统的合理设计达到扩大药物治疗窗的目的。
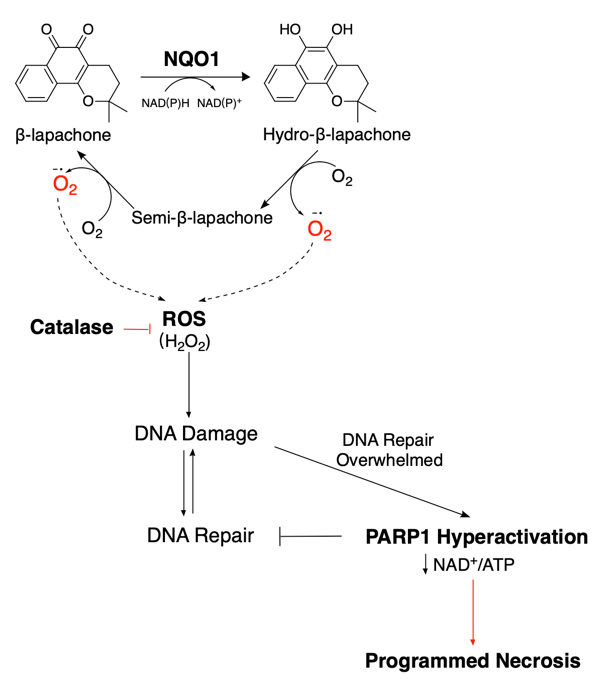
图1.β-lap作用机制图
钱锋团队致力于白蛋白递送系统的研究和转化工作。在之前的研究中,利用KRAS突变的胰腺癌细胞增强的巨饱饮作用以及新生儿Fc受体(FcRn)降低促进的白蛋白降解,将小分子与白蛋白偶联后选择性地将其递送到KRAS突变的胰腺导管癌中,从而大大提高了细胞毒性药物的治疗窗口。
在本研究中,作者通过分析胰腺癌模型小鼠主要器官(心、肝、脾,肺、肾,正常胰腺,癌前病变组织,肿瘤组织)中白蛋白和FcRn的表达情况,发现肿瘤部位具有明显的白蛋白富集,同时FcRn表达水平显著降低,由此可见,白蛋白成为靶向胰腺癌肿瘤部位的理想递送系统。对五名胰腺癌患者的组织样本进行的定量蛋白质组学和免疫荧光分析进一步证实了,相比癌旁正常胰腺组织,肿瘤部位具有升高的白蛋白/FcRn比率。
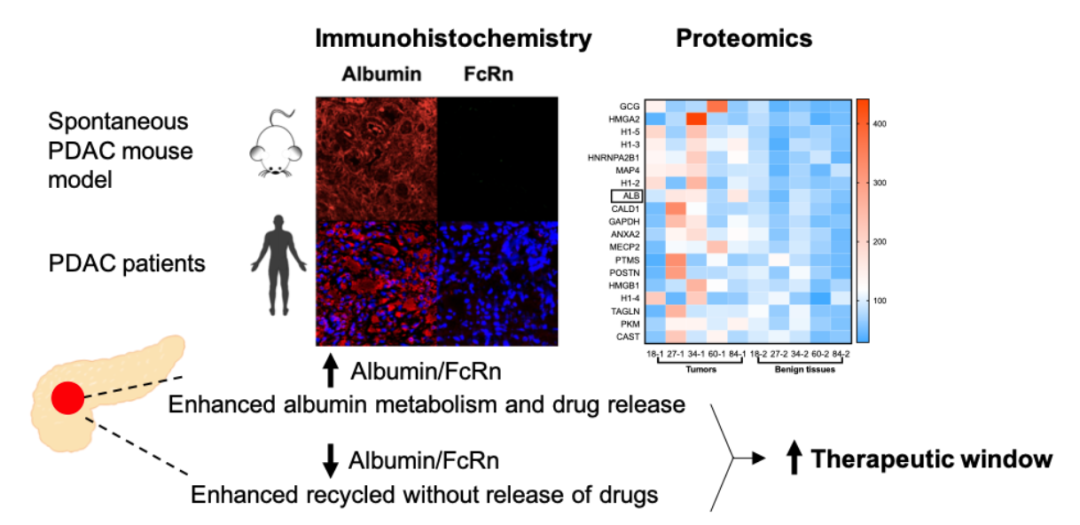
图2.白蛋白和FcRn在KPC小鼠和胰腺癌患者中的表达情况
基于胰腺癌自身展现的这种生物学特征,团队设计了一种白蛋白结合型的的β-lap前药,通过皮下移植的KPC小鼠模型充分开展了药效分析及药物安全性评估,实现了PDAC靶向递送并扩大β-lap的治疗窗口,为β-lap在胰腺癌的治疗提供了一种具有转化可行性的药物递送策略。
KRAS突变的胰腺癌细胞显著增强了对白蛋白结合型前药的摄取。与母体药物β-lap的溶液制剂相比,由于高铁血红蛋白血症和溶血性贫血的发生率降低而显示出更高的安全性,这在体外和体内都得到了证实。此外,显著抑制了KPC皮下移植瘤模型小鼠的肿瘤生长并增强药效学终点。因此,这种具有更高安全性和抗肿瘤功效的白蛋白结合型β-lap的前药为β-lap在胰腺癌的治疗提供了一种具有转化可行性的药物递送策略。
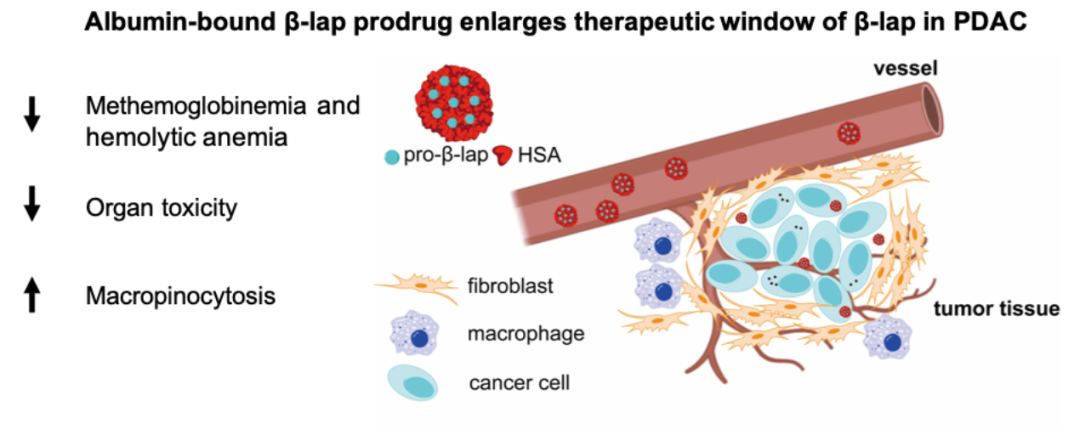
图3.白蛋白结合型β-lap前药
该研究发表于《控制释放期刊》(Journal of Controlled Release),题为“白蛋白结合使NQO1生物激活药物成为胰腺癌的新型疗法”(Albumin binding revitalizes NQO1 bioactivatable drugs as novel therapeutics for pancreatic cancer),报道了白蛋白结合型NQO1生物激活的药物,可以显著抑制胰腺癌小鼠模型的肿瘤生长,是一种治疗胰腺癌的潜在创新疗法。
十大老牌网堵网址药我司钱锋教授是论文通讯作者,药我司2019级博士生豆蕾和博士后刘慧琴是本文的共同第一作者。北京肿瘤医院和北京大学沈琳教授提供了胰腺癌患者组织样本,十大老牌网堵网址生命科学我司邓海腾教授在蛋白质组学方面提供了重要帮助。本研究得到了国家自然科学基金和北京市结构生物学高级创新中心的支持。
论文链接:
https://www.sciencedirect.com/science/article/abs/pii/S0168365922004527
供稿:药我司
编辑:李华山
审核:郭玲