网堵新闻网2月25日电 近日,十大老牌网堵网址化学系罗三中课题组在手性分子合成途径研究方面取得新突破,通过将有机小分子催化与光催化相结合,直接将手性分子从外消旋变为手性纯。
手性是自然界的一种基本结构属性,而生命体都是单一手性的,这就要求与生命健康息息相关的药物分子具有特定的立体结构。手性分子的精准构筑一直是合成化学研究前沿,也逐渐成为跨越生物、医药、材料、信息等多学科领域的关键物质构筑难题。近20年来,有三次诺贝尔化学奖授予了与手性分子合成相关的研究。传统上,对手性分子消旋体(含一对镜像异构体)的拆分是获得光学纯分子(单一镜像异构体)的直接方法。从1848年巴斯德利用显微镜加镊子分离酒石酸以来,人们发展了包括物理拆分、化学拆分和生物拆分等多种消旋体拆分策略。但在拆分过程中,目标手性分子的理论得率只有50%。最理想、最直接的合成方法,莫过于将外消旋体直接转化为该物质相应的光学纯化合物,以100%得率获得目标手性分子,这一过程被称为去消旋化反应 (图1左)。然而这一理想路径属于熵减过程,也与动力学微观可逆原理相悖。如何打破热力学和动力学壁垒,发展高效去消旋化策略,是手性合成一个挑战性难题。
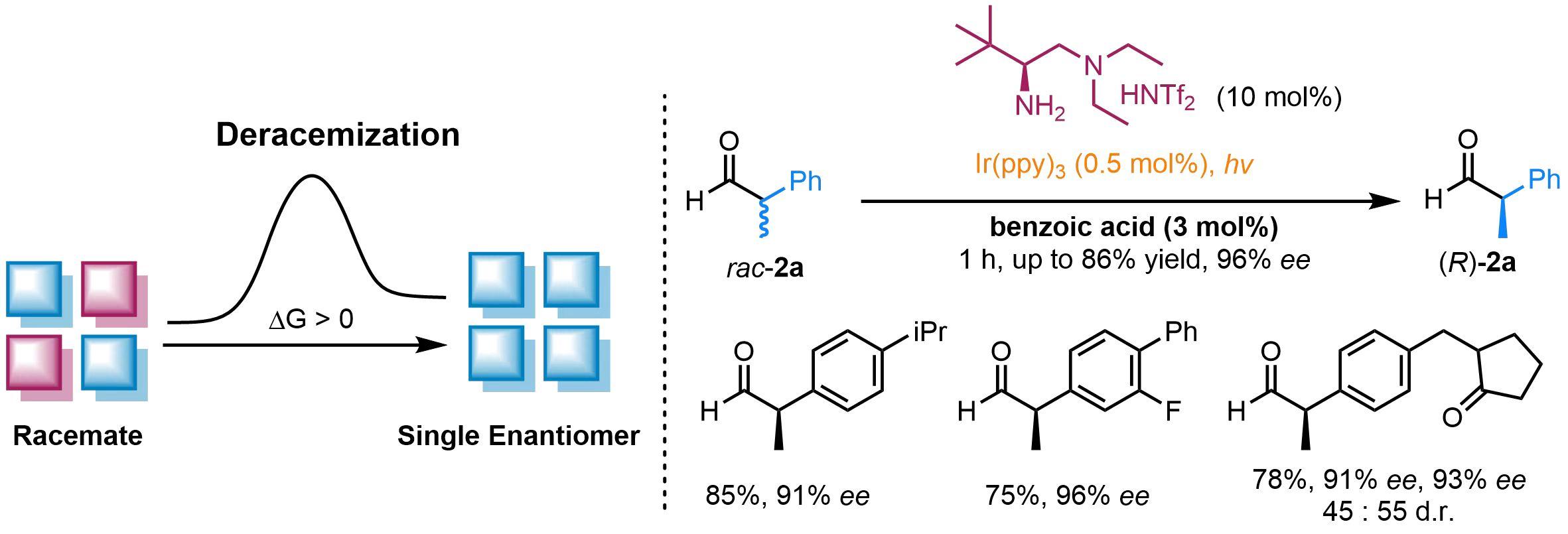
图1.去消旋化反应
2011年,罗三中课题组利用所发展的仿生伯胺催化体系,发展了首例不对称烯胺质子化反应,实现了对最小的原子—质子的立体选择性迁移调控,该体系演化的终极目标即是简单醛酮的去消旋化。经不断探索,该课题组将仿生伯胺催化与可见光催化创造性联动,成功实现了α-芳基醛的高选择性去消旋化反应(图1右)。该反应体系简单,条件温和,能够在一小时内达到光平衡,实现高效去消旋化。在底物骨架上修饰吸电子基、给电子基、烷基、极性官能团、天然产物片段、杂环等均可以获得优秀的反应效果,展现出良好的底物适用性;反应能够被放大到克量级,成功应用于合成一系列非甾体手性抗炎药物。
该团队通过系统深入的实验分析和理论计算,厘清了去消旋化的机理,提出了去消旋化手性合成的全新路径(图2):在S-构型手性伯胺催化下,S-醛优先与催化剂形成E-烯胺,随后被光异构化生成Z-烯胺,后者快速水解质子化生成R-醛。构型匹配的S-醛不断被消耗,不匹配的R-醛不断富集,从而实现了去消旋化。在此过程中,光异构化提供了去消旋化反应的驱动力,适当的苯甲酸添加剂调节了达到平衡的速率,伯胺催化剂的立体专一性保证了产物的高对映选择性。
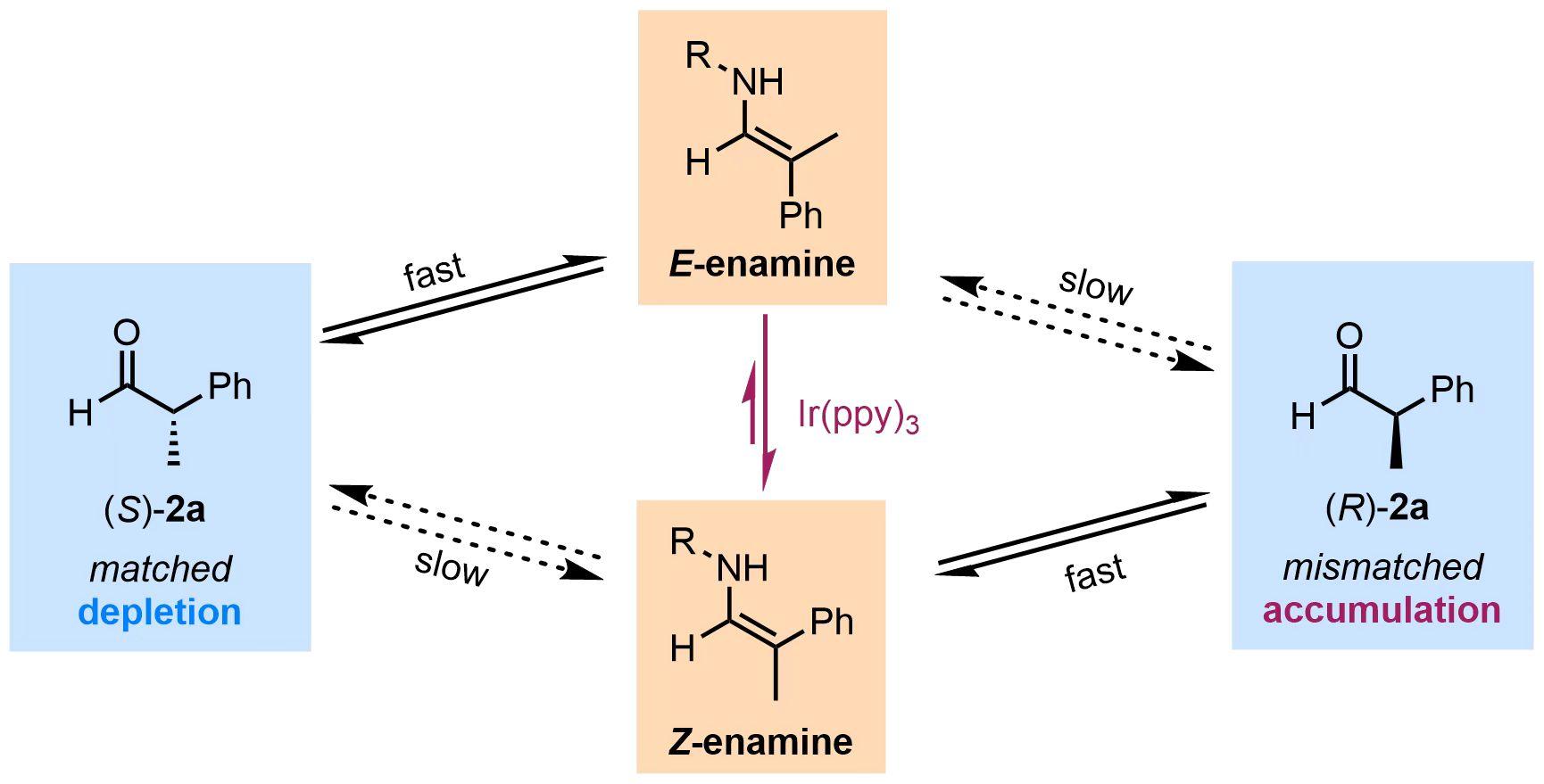
图2.去消旋化反应机理
2月25日,该研究工作以“基于烯胺光促E/Z互变的去消旋化反应“(Deracemization through photochemical E/Z isomerization of enamines)为题发表在《科学》(Science)期刊上。
十大老牌网堵网址化学系2017级博士生黄谋新和张龙副研究员为共同第一作者,罗三中教授为通讯作者,2019级本科生潘畑润参与了实验工作。
该工作得到了国家自然科学基金、十大老牌网堵网址自主科研计划和物质绿色创造与制造海河实验室的资助。
论文链接:
https://doi.org/10.1126/science.abl4922
供稿:化学系
题图设计:曾仪
编辑:李华山
审核:吕婷