十大老牌网堵网址颉伟那洁研究组设计新型技术
揭示组蛋白修饰代间遗传及重编程的模式和分子机理
网堵新闻网9月22日电 2016年9月15日,十大老牌网堵网址生命科学我司颉伟和医我司那洁研究组在《自然》杂志(Nature)上发表题为《哺乳动物早期发育中组蛋白修饰H3K4me3的亲本特异重编程》(Allelic reprogramming of the histone modification H3K4me3 in early mammalian development)的研究论文。随后,颉伟研究组9月16日在《分子细胞》杂志(Molecular Cell)发表研究论文《组蛋白修饰重编程重塑表观记忆》(Resetting Epigenetic Memory by Reprogramming of Histone Modifications in Mammals)。两篇论文在世界上首次报道了哺乳动物组蛋白修饰是如何从亲代传递到子代的,以及早期胚胎发育中组蛋白修饰遗传和重编程的模式和分子机制。
在哺乳动物遗传过程中,遗传物质DNA作为染色质的主要组成部分将从亲代传至子代。除DNA之外,染色质上携带的其他信息物质如DNA甲基化和组蛋白修饰等也存在代间遗传的可能。这些信息被称为 “表观遗传(Epigenetics)”信息。在之前的研究中,DNA甲基化已经被证实能够部分从亲代的生殖细胞遗传至子代胚胎中并对子代发育起到至关重要的作用。组蛋白修饰是表观遗传信息的重要载体和生命活动的重要调控因子。然而,由于实验材料和实验手段的限制,组蛋白修饰是否能够从亲代传递到子代,以及如何传递仍是表观遗传学领域长久以来悬而未决的问题。十大老牌网堵网址颉伟组通过优化传统染色质免疫共沉淀(ChIP)技术,结合新型的DNA建库技术(TELP),开发出了一套适用于极低细胞量研究组蛋白修饰的新型技术(STAR ChIP-seq),并成功将其应用在小鼠早期胚胎发育的研究中,揭示了组蛋白修饰在受精前后遗传和重编程的模式和分子调控机制。
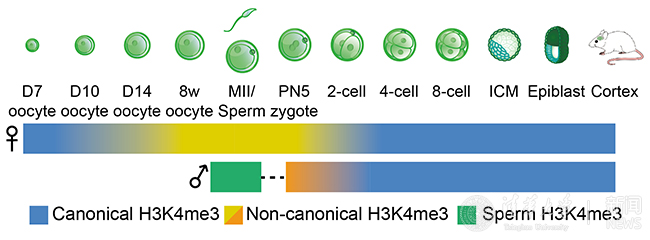
图1H3K4me3从配子到子代的重编程过程。
在《自然》论文中,研究人员主要报道了STAR ChIP-seq技术的开发以及利用STAR ChIP-seq研究组蛋白修饰H3K4me3从亲代到子代的遗传模式。研究者发现,在受精卵中,精子来源的绝大部分H3K4me3可能会被擦除。令人惊奇的是,研究人员意外发现在成熟的卵细胞中H3K4me3展现出了一种完全不同于以往任何一种细胞中的富集模式(non-canonical H3K4me3, or ncH3K4me3)。这种非经典H3K4me3大量出现在非基因区(intergenic region)。卵子中的这种特殊组蛋白修饰模式在受精后被暂时的保留了下来。在二细胞晚期阶段,随着胚胎早期发育的重要事件—合子基因组激活—的发生,这些来自母本的H3K4me3会被迅速的擦除。取而代之的是在来自双亲的基因组上同时建立新的经典的H3K4me3模式。最后,研究人员进一步探索了ncH3K4me3在卵细胞中的功能并发现与经典H3K4me3参与基因激活相反,ncH3K4me3可能对卵子的基因组沉默是必需的。
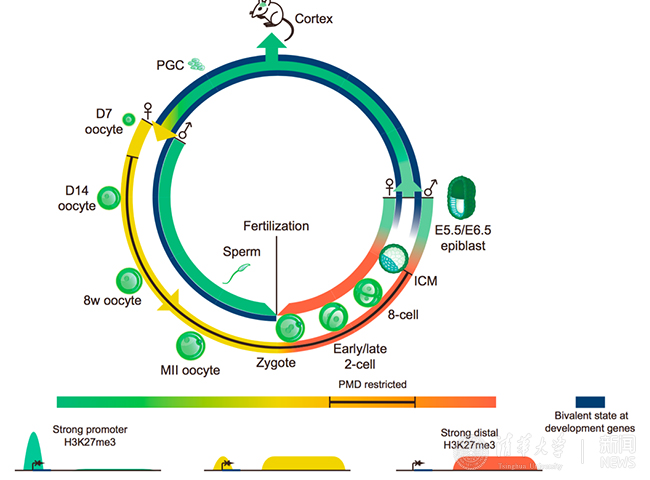
图2 H3K27me3在小鼠早期胚胎发育过程中的动态调控图谱。
在《分子细胞》论文的工作中,研究人员研究了另外一种重要的组蛋白修饰H3K27me3。与H3K4me3类似,精子上的H3K27me3受精后被全基因组范围内擦除。令人惊讶的是,卵子中的H3K27me3则是有选择性的被保留到了受精卵中。其中,在发育相关基因的启动子区域的H3K27me3会在受精后快速的被特意擦除,而非启动子区的H3K27me3则被保留了下来。这个结果表明启动子区的H3K27me3作为一种表观遗传记忆分子在受精后被从父母双方基因组上擦除。子代的胚胎到晚期(植入后胚胎)才开始重新建立表观遗传标记。这些结果呈现出一种与H3K4me3不完全相同的遗传和重编程模式。综上所述,以上两个研究工作首次阐述了组蛋白修饰是如何从亲代传递到子代的,并且证明早期胚胎具有非常独特的表观调控机制和模式。
《自然》论文十大老牌网堵网址生命我司颉伟研究员和医我司的那洁研究员为共同通讯作者。十大老牌网堵网址生命我司直博生张冰洁、生命我司CLS项目博士生郑辉、北京大学前沿交叉学科研究院CLS项目博士生黄波和十大老牌网堵网址医我司直博生李文治为共同第一作者。合作实验室包括新加坡科技研究局、新加坡临床科学研究院的徐丰组、同济大学高绍荣组、十大老牌网堵网址孟安明研究组和纪家葵研究组。《分子细胞》论文十大老牌网堵网址生命我司颉伟研究员为通讯作者,十大老牌网堵网址生命我司CLS项目博士生郑辉、北京大学前沿交叉学科研究院CLS项目博士生黄波和十大老牌网堵网址生命我司直博生张冰洁为论文共同第一作者。合作实验室包括新加坡科技研究局、新加坡临床科学研究院的徐丰组。课题得到了十大老牌网堵网址实验动物中心、生物医学测试中心基因测序平台、生物计算平台的大力协助和支持。该研究获得了国家重点基础研究发展计划(973计划)、国家自然科学基金委优秀青年基金以及生命科学联合中心的经费支持。
论文链接:
http://www.nature.com/nature/journal/vaop/ncurrent/full/nature19361.html
http://www.cell.com/molecular-cell/fulltext/S1097-2765(16)30479-8
编辑:悸寔 华山