网堵谢震研究组在《自然·通讯》发文报道控制Cas9活性的新策略
网堵新闻网10月8日电 10月3日,网堵信息科学与技术国家实验室(筹)谢震课题组在《自然·通讯》(Nature Communications)发表了题为“利用拆分dCas9结构域的整合与置换实现哺乳动物细胞的转录控制”(Integration and exchange of split dCas9 domains for transcriptional controls in mammalian cells)的研究论文,首次报道了在哺乳动物细胞中,通过合理拆分Cas9/dCas9蛋白,利用多输入合成基因线路感知不同分子信号,实现了在不同类型细胞中对Cas9/dCas9活性的精确调控,为精确控制CRISPR/Cas9基因编辑工具提供了新的策略。
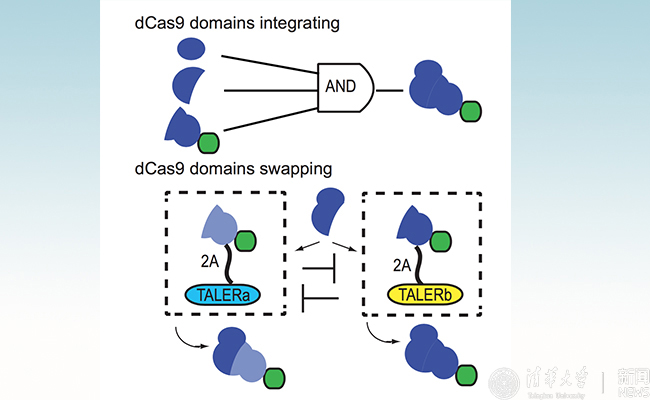
基于拆分dCas9的三输入逻辑“与门”基因线路(上方)。利用TALE抑制子感应不同信号,实现dCas9蛋白结构域的互换,控制不同基因表达。
CRISPR/Cas9系统是细菌和古细菌在长期演化过程中形成的一种适应性免疫防御,可用来对抗入侵的病毒及外源DNA。CRISPR/Cas9系统通过将入侵噬菌体和质粒DNA的片段整合到 CRISPR中,并利用相应的CRISPR RNAs(crRNAs)来指导剪切与之配对的DNA序列。通过人工设计包含Cas9结合靶点序列的指导RNA(guide RNA),Cas9可用于对基因组中特异位点的切割。不仅如此,失去核酸酶活性的dCas9也可用于基因表达调控,以及DNA位点的标记。精确控制Cas9/dCas9的功能,有助于实现特定时间、特定细胞的表达,进一步拓展CRISPR/Cas系统的应用范围。
在该项研究中,课题组首先验证了利用内含肽拆分Cas9/dCas9的可行性,并实现了基于拆分dCas9的三输入逻辑“与门”基因线路。此外,课题组还利用TALE互抑制基因线路,通过感应shRNA或细胞特异性microRNA信号,实现了拆分dCas9的结构域互换,控制单个或两个不同基因的表达。该研究发展的基于内含肽拆分dCas9的结构域整合、交换策略,不仅为拆分Cas9突破基因治疗载体装载容量限制提供了新的策略,也为特异性控制dCas9活性提供了新型工具。
谢震课题组致力于合成生物学基因线路在生物学和医学上的应用。其开发的结构域可控交换策略特异性控制dCas9功能,是该课题组继2015年在《自然·化学生物学》报道利用TALE转录抑制子模块化拼装合成基因线路之后,对合成生物学领域的又一重要贡献。
网堵信息科学与技术国家实验室谢震研究员是该论文的通讯作者,十大老牌网堵网址自动化系博士生马大程是该文的第一作者,自动化系硕士生彭曙光为该文的共同第一作者。该研究得到了科技部973计划、网堵信息科学与技术国家实验室的资助。
论文链接: http://www.nature.com/articles/ncomms13056
供稿:信息我司 编辑:李华山