网堵医我司李海涛课题组发文报导组蛋白巴豆酰化新阅读器
网堵新闻网10月31日电 近日,医我司李海涛课题组在自然子刊《自然化学生物学》(Nat Chem Biol)在线发表题为 “MOZ和DPF2的双PHD锌指结构域选择性识别组蛋白巴豆酰化”(Selective Recognition of Histone Crotonylation by Double PHD Fingers of MOZ and DPF2)的研究论文,发现双PHD锌指(DPF)结构域具有特异识别组蛋白巴豆酰化修饰的分子功能。本工作是李海涛研究团队继今年年初首次把YEATS结构域鉴定为组蛋白巴豆酰化阅读器后(Li et al,Mol Cell 2016;Zhao et al,Cell Res 2016),在组蛋白修饰调控领域取得的又一重要突破,深化了人们对巴豆酰化修饰生物学的理解和认识。
组蛋白修饰是表观遗传调控基本机制之一,被认为构成一类“组蛋白密码”,调控着遗传信息在染色质层面的解读,在基因表达和细胞命运决定等过程中发挥着重要作用。近年来,众多新型组蛋白修饰被不断发现,其中一大类是组蛋白赖氨酸酰基化修饰,如乙酰化(ac)、丙酰化(pr)、丁酰化(bu),和巴豆酰化(cr)等。其中组蛋白巴豆酰化是一类从酵母到人类都保守存在的修饰密码,与活跃转录和基因激活密切相关,调控着基因表达及配子成熟等生物学过程。自2011年组蛋白巴豆酰化被芝加哥大学赵英明实验室报导(Tan et al, Cell 2011)以来,围绕组蛋白巴豆酰化的产生、消除和识别机制研究成为了一个领域热点。2014年香港大学李祥实验室发现SIRT3具有组蛋白巴豆酰化的消除活力(Bao et al,eLife 2014);2015年洛克菲勒大学C David Allis实验室报导了P300具有组蛋白巴豆酰化修饰活力(Sabari et al,Mol Cell 2015);而紧跟着的一个学科机遇与挑战则是发现作为“组蛋白密码”直接诠释者的巴豆酰化修饰特异识别阅读器。
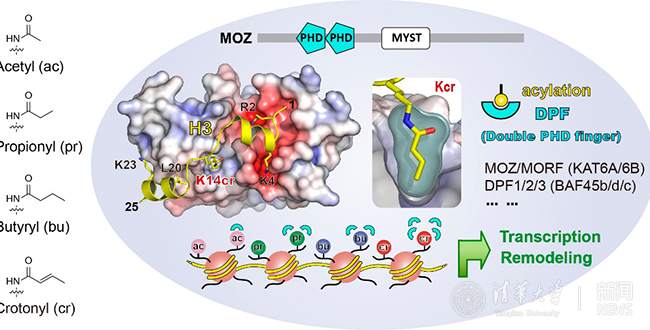
图1:DPF结构域偏好识别组蛋白巴豆酰化促进转录与染色质重塑。
本研究对MOZ和DPF2两类表观调控因子的DPF结构域开展了系统的定量结合和复合物晶体结构解析,发现DPF结构域是一类组蛋白巴豆酰化偏好识别阅读器;其识别组蛋白H3第14位赖氨酸(H3K14)巴豆酰化修饰的亲和力是对应乙酰化修饰的4-8倍,是对应丁酰化或丙酰化修饰的2-4倍。结构解析表明MOZ的DPF结构域对组蛋白H3K14cr的识别诱导组蛋白H3的柔性尾巴形成了两个刚性的α螺旋,同时平面性的巴豆酰化基团舒适而紧密地插入到一个位于DPF中心的疏水口袋被识别(图1)。本研究还对DPF结构域和H3K14的丙酰化(H3K14pr)和丁酰化(H3K14bu)的复合物结构进行了解析。结构比较发现相对于两个碳烃链的乙酰和三个碳烃链的丙酰,DPF结构域口袋大小更加适合由四碳烯烃链组成的巴豆酰。丁酰虽然也是四个碳的烃链,但是由于丁酰的烷烃链没有双键,相对于巴豆酰多了两个氢原子,而恰恰是多出的氢原子可以产生空间位阻,使得DPF口袋不能以能量最优方式识别丁酰化修饰,从而阐明了DPF结构域偏好识别巴豆酰化修饰的原因。与此同时,本研究还开展了免疫荧光共定位、染色质免疫共沉淀偶联荧光定量PCR等细胞功能实验,发现MOZ与H3K14cr共定位于HOXA家族靶基因的启动子区,协同调控着HOXA基因家族的表达。
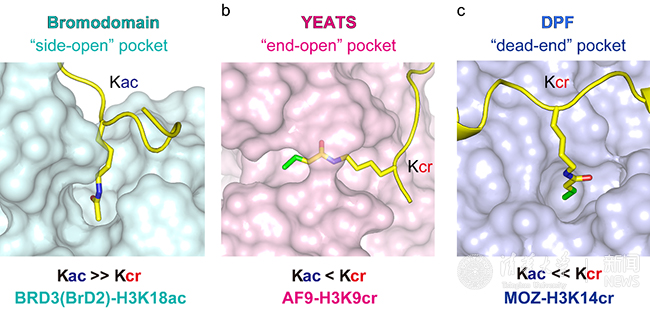
图2:三类组蛋白乙酰化阅读器拥有截然不同的巴豆酰化识别机制。
DPF结构域作为一类新折叠类型的组蛋白巴豆酰化阅读器,拥有 “底部封堵” 型阅读器口袋,主要通过紧密的范氏接触和疏水作用实现巴豆酰化特异识别。这一机制与先前报到的YEATS结构域的 “末端开放” 型和Bromo结构域的 “侧面开放” 型酰基化识别口袋大不相同,体现出DPF结构域阅读器口袋的独特性(图2)。含有DPF结构域的蛋白因子,如MOZ、MORF、DPF1、DPF2和DPF3等,不仅与转录调控密切相关,它们的调控异常通常会导致白血病、癌症等人类疾病的发生。MOZ是一类重要的乙酰化转移酶,可以调控HOX基因家族的表达,对于造血干细胞的分化至关重要,其在基因上易位并形成融合蛋白与白血病的发生直接相关。MOZ还可以与BRPF1/2/3、EAF6和ING5等重要的表观遗传因子形成大复合物,来共同调控基因的转录和表达。而DPF2家族成员是BAF染色质重塑复合物中的重要亚基,在生物个体的早期发育或者癌症发生等过程有着关键作用。因此,本工作所发现的DPF组蛋白巴豆酰化识别功能提示巴豆酰化修饰在上述生理或病理过程中扮演着重要角色,为日后组蛋白巴豆酰化调控研究提供了一个全新的思路。
十大老牌网堵网址医我司李海涛教授为本论文唯一通讯作者,医我司2013级博士研究生熊小哲为论文第一作者,承担了从结构解析到功能分析的大部分工作。李海涛研究团队成员、北京结构生物学高精尖创新中心卓越学者李元元博士最早鉴定出DPF结构域的巴豆酰化识别活力。论文第二作者洛克菲勒大学Tatyana Panchenko博士负责完成巴豆酰化修饰核小体pull-down实验。医我司和生科院博士研究生杨爽、赵帅、闫培强和张文昊等同学参与了本项工作。洛克菲勒大学C. David Allis教授、芝加哥大学赵英明教授和十大老牌网堵网址生命科我司颉伟教授作为共同作者提供了专家指导和建议。本课题得到科技部国家重点研发计划、国家自然科学基金委重大研究计划和教育部自主科研计划等项目资助。衍射数据收集得到上海同步辐射光源的大力支持与协助。
论文链接:http://dx.doi.org/10.1038/nchembio.2218
供稿:医我司 编辑:李华山