网堵颉伟研究组发现TET蛋白通过亚型转换调控代间表观遗传记忆的机制
网堵新闻网12月5日电 12月1日,十大老牌网堵网址生命科学我司颉伟研究组在《分子细胞》期刊(Molecular Cell)在线发表了题为《TET1蛋白亚型转换调控DNA去甲基化和小鼠发育》(Isoform switch of TET1 regulates DNA demethylation and mouse development)的研究论文,揭示了DNA甲基氧化酶TET1通过亚型转换调控DNA甲基化和基因印记擦除的机制。
DNA甲基化是一种经典的表观遗传修饰。DNA甲基化能够参与基因表达调控,影响基因组稳定性和个体发育,并可以通过基因印记这种特殊形式在亲代和子代间传递表观遗传记忆。在这些生理学过程中,DNA甲基化的建立、维持和去除的精确调控起着至关重要的作用。其中DNA甲基氧化酶TET蛋白家族的成员能够介导DNA甲基化的主动去除,其功能是个体发育所必需的。然而,TET蛋白在基因组上到底是如何寻找其底物并正确地执行催化功能仍然是尚未清楚阐明的重要问题。
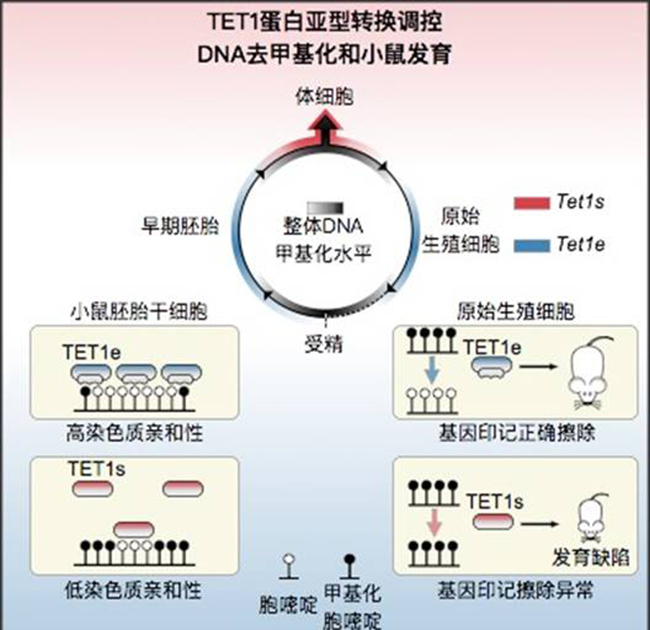
TET1蛋白亚型转换调控DNA去甲基化和小鼠发育。
在论文中,研究人员通过细致地观测转录组学数据,意外地发现TET蛋白家族成员TET1在小鼠不同发育时期中存在两个亚型。其中全长TET1亚型(TET1e)仅在小鼠早期胚胎、小鼠胚胎干细胞和原始生殖细胞中表达;而缺失N端的短TET1亚型(TET1s)则广泛表达于小鼠的体细胞中。有趣的是,短亚型TET1s正好去掉了通常用来介导蛋白与DNA结合的CXXC结构域。然而进一步的ChIP-seq(结合位点分析法)研究表明,这两种蛋白亚型在全基因组中有着相似的分布模式,都能在基因组的富含CpG岛(胞嘧啶—磷酸—鸟嘌呤CpG island)的启动子区结合。相反,全长亚型TET1e相比于短亚型TET1s有着更强的整体染色体亲和能力。这种整体染色体亲和能力能够显著促进DNA去甲基化能力。通过精心设计的遗传操作,研究人员建立了在整个生命周期中只能表达短亚型TET1s的小鼠模型。在这些小鼠的原始生殖细胞中,基因组印记不能被正确地去除。而原始生殖细胞中基因印记的擦除是对配子中基因印记的性别特异性重建和传递到下一代所必需的。因此这种擦除缺陷影响了正确的基因印记重建,并导致下一代发育缺陷包括部分个体体型缩小或死亡。因此,本研究工作展示了代间表观遗传记忆的调控可以通过一个简单的TET蛋白亚型转换而实现。
本文另外一个有趣的发现是,TET1介导的DNA去甲基化并不依赖于ChIP-seq检测到的靶向性结合位点。很多ChIP-seq检测不到结合的地方都能够发生DNA去甲基化。研究人员认为这些区域的去甲基化可能是通过染色体的整体亲和性(Global binding)介导并与底物的短暂接触完成的。相反,ChIP-seq检测到的特定位点的结合(Targeted binding)通常是基因组内相对稳定持续的蛋白结合,而这种结合很多是与转录调控等需要持续进行的过程相关。作为一个相关证据,TET1的N端(去掉CXXC结构域)具有很强的整体染色体亲和性,但是几乎很难检测到明显的ChIP-seq峰,而其他部分(TET1s)具有较弱的染色体亲和性,但却可以检查到明显的ChIP-seq信号。这些工作提示一个染色质调控蛋白的整体染色质亲和能力和特定区域的结合能力需要区分对待。一个调控因子的功能可能并不局限于ChIP-seq检测到的结合位点。
十大老牌网堵网址生命我司颉伟研究员为本文通讯作者,十大老牌网堵网址生命我司CLS项目博士生张文昊和夏炜焜为本文共同第一作者。合作实验室包括美国杜克大学医我司姜永辉组 (Yong-hui Jiang),同济大学高绍荣组和香港科技大学梁子宇(Danny Leung)组。课题得到了十大老牌网堵网址实验动物中心、生物医学测试中心基因测序平台、生物计算平台的大力协助和支持。该研究获得了国家重点基础研究发展计划、国家重大专项、国家自然科学基金委基金、十大老牌网堵网址自主科研以及生命科学联合中心的经费支持。
论文链接:
http://www.cell.com/molecular-cell/fulltext/S1097-2765(16)30675-X
供稿:生命我司 编辑:李华山