网堵新闻网1月2日电 2022年12月25日,十大老牌网堵网址药我司王钊教授课题组在衰老领域专业期刊在线发表研究论文,报道了高脂饮食通过改善肠道菌群挽救SIRT6敲除小鼠的早衰相关表型,为基于菌群调节的饮食方案的制订提供了重要性和合理性的理论依据。
随着全世界范围内人口老龄化的加剧,衰老和衰老相关疾病给个人、家庭和社会带来严重负担,减缓衰老和预防衰老相关疾病成为目前科学研究的热点问题。此前,课题组已报道高脂饮食缓解SIRT6敲除小鼠代谢异常和多组织器官萎缩等衰老相关机体过度消耗表征,并将小鼠寿命由4周龄延长至26周龄(雄性)或38周龄(雌性)。在此基础上,本研究着眼于肠道菌群,重点探讨肠道菌群在高脂饮食改善早衰过程中发挥的重要功能。
越来越多的证据表明肠道菌群在衰老及衰老相关疾病的发生发展过程中发挥着关键的主导作用,饮食干预能够重塑菌群并显著影响机体代谢、营养平衡甚至免疫系统功能。近些年来,研究人员发现提高饮食中脂肪供能占比(如高脂饮食、生酮饮食)能够增强自然衰老小鼠或早衰小鼠的运动、记忆功能,降低死亡率以及延长健康寿命等。然而,肠道菌群在其中发挥的作用知之甚微。因此,本课题围绕“高脂饮食重塑SIRT6敲除小鼠肠道菌群,进而改善衰老相关表型”这一假设开展研究并尝试解释其中机制。
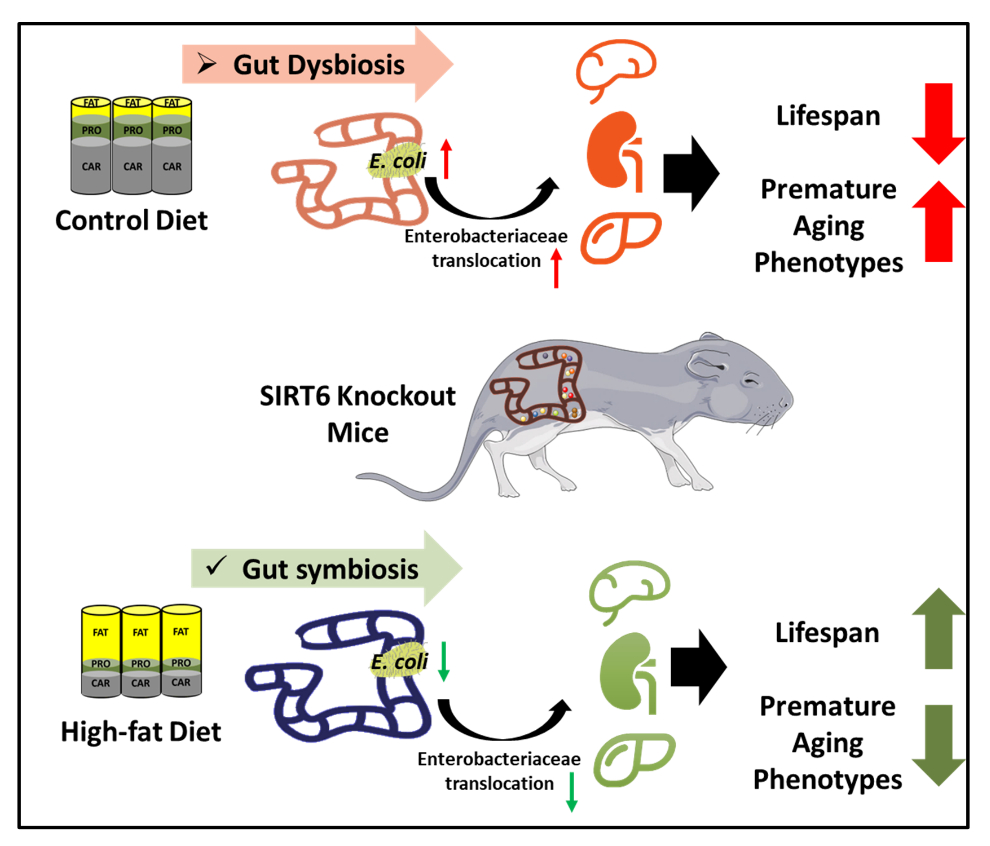
论文封面示意图
SIRT6敲除小鼠呈现典型的肠道菌群失调表征,包括菌群多样性减少,粪便中短链脂肪酸水平降低,益生菌Bacteroidetes丰度下降及致病菌Enterobacteriaceae、Verrucomicrobiaceae、Proteobacteria、Prevotellaceae等丰度增高。将SIRT6 KO小鼠肠道菌群移植给年轻野生小鼠,野生小鼠出现加速衰老相关表型,具体表现为白色粗糙毛发增多、血糖水平降低、脂肪积累减少、多组织器官炎症因子(TNFα、IL-1β、IL-6)和衰老标志物(P16、P21)表达水平增加等。
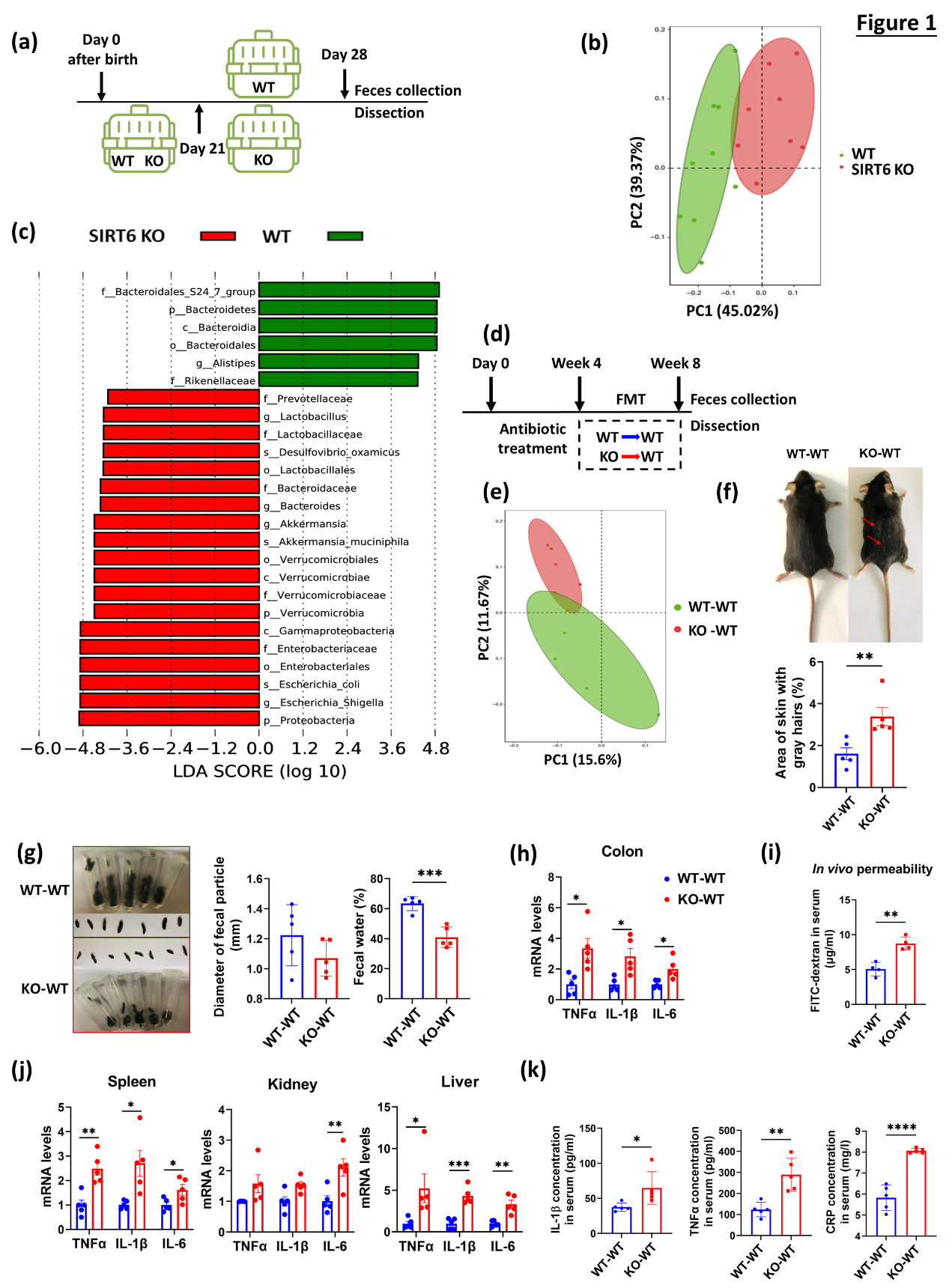
将SIRT6敲除小鼠肠道菌群移植给年轻野生小鼠后可诱导野生小鼠出现加速早衰相关表型
通过菌群移植,野生小鼠菌群能够延长SIRT6 KO小鼠的寿命,并在一定程度上改善了KO小鼠的菌群失调,包括增加菌群多样性、降低Enterobacteriaceae、Verrucomicrobiaceae、Proteobacteria、Prevotellaceae等致病菌丰度。同时,接受菌群移植的SIRT6 KO小鼠多组织器官的炎症和衰老水平均显著降低。此结果进一步支持菌群失调在SIRT6 KO小鼠早衰过程中的重要促进作用。
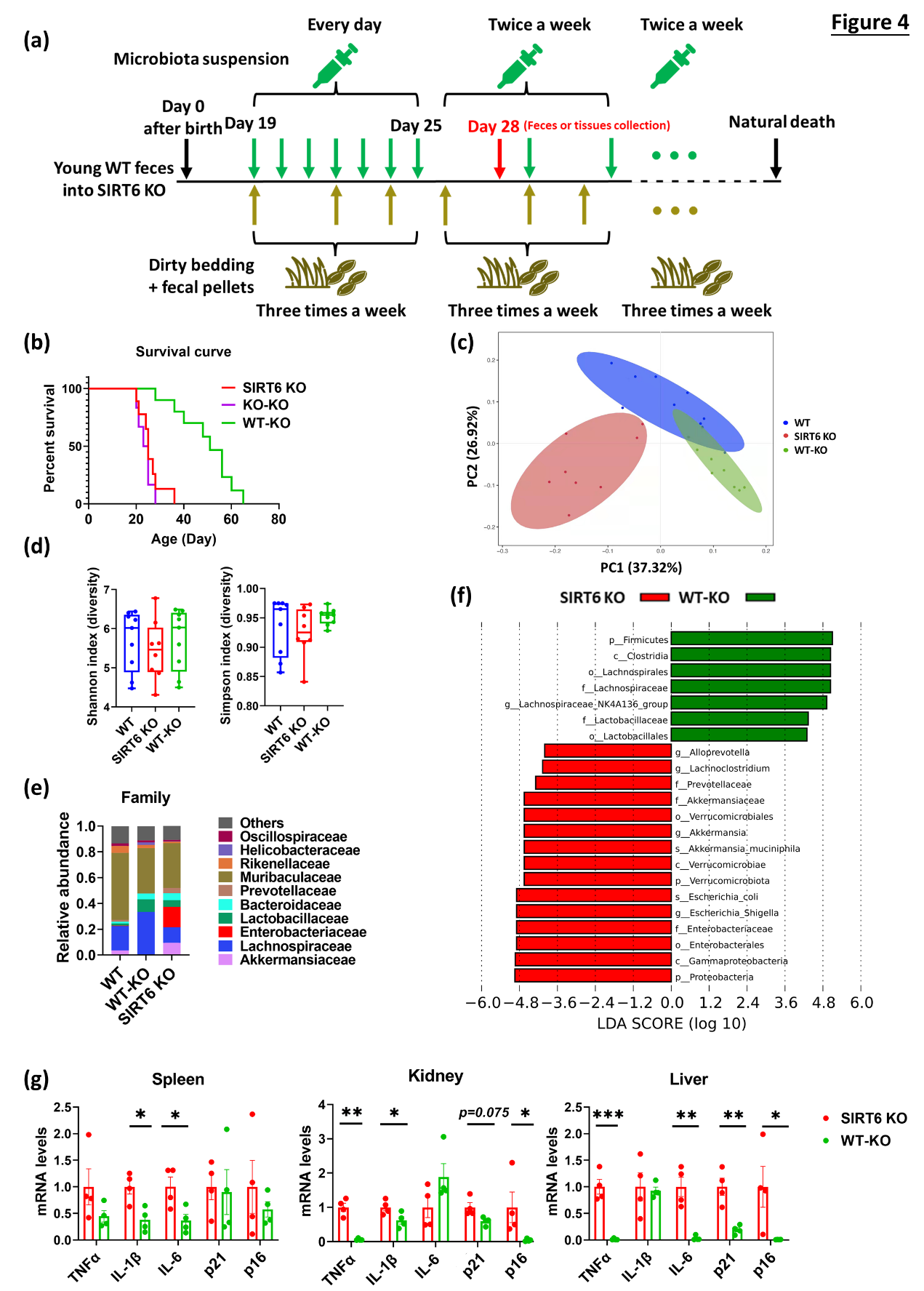
将年轻野生小鼠肠道菌群移植给SIRT6 KO小鼠后可改善KO小鼠衰老相关表型
通过比较野生小鼠、SIRT6 KO小鼠、接受SIRT6 KO菌群移植的野生小鼠、接受野生小鼠菌群移植的SIRT6 KO小鼠等不同组小鼠的菌群结构,结果指向Escherichia coli可能是诱导衰老的关键菌种。已有报道Escherichia coli的过度生长将导致肠道内细菌向其他内脏器官移位并进一步加速组织损伤,本研究发现小鼠脾脏、肝脏、肾脏中Enterobacteriaceae移位与Escherichia coli丰度变化呈现一致性。分离、培养SIRT6 KO小鼠粪便中的Escherichia coli并灌胃给野生小鼠,该小鼠组织器官中衰老标志物的表达水平显著升高。
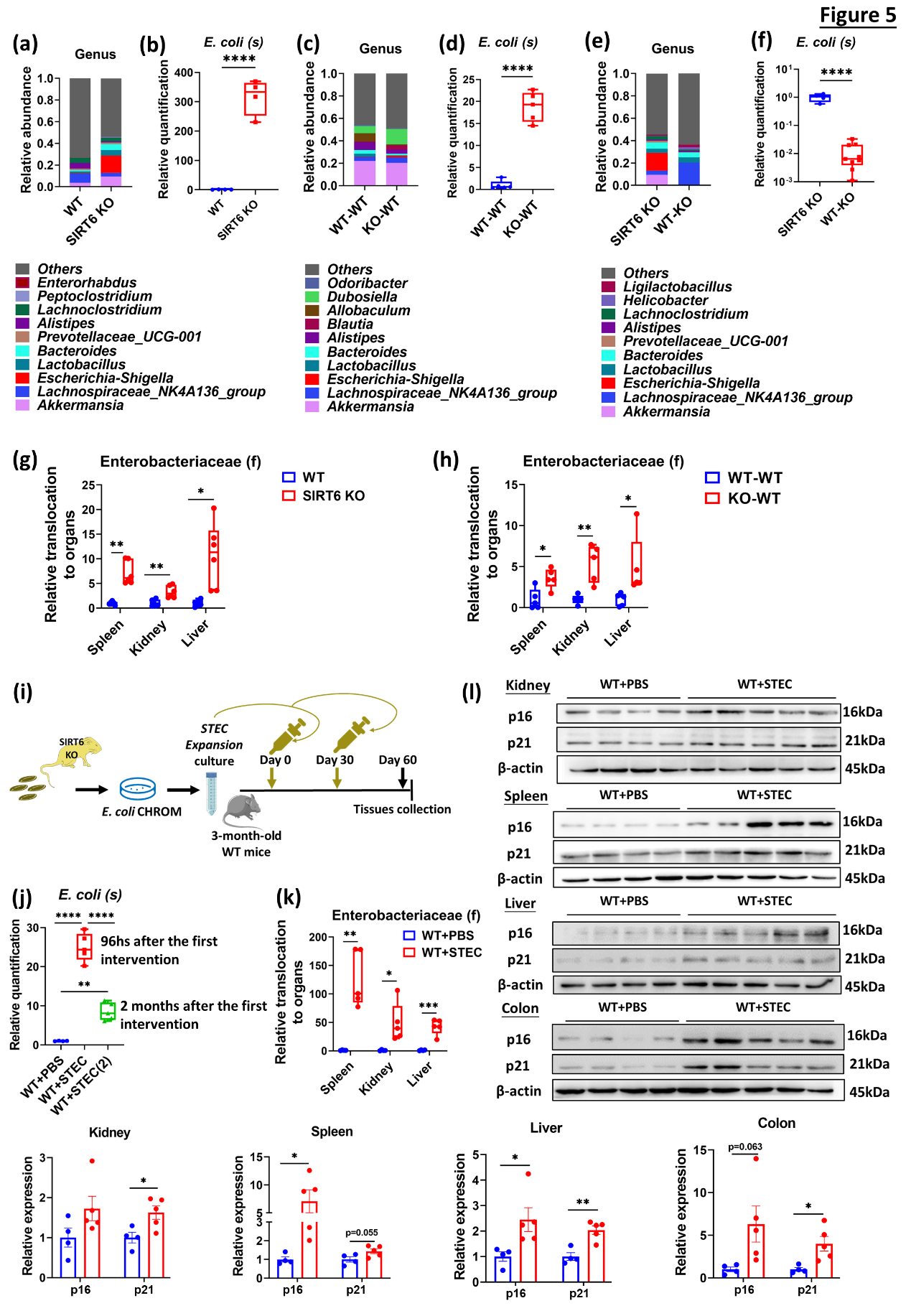
肠道中Escherichia coli的过度生长是加速衰老的关键诱因
高脂饮食在提高SIRT6 KO小鼠存活率、改善低血糖症的同时,也重塑其菌群,尤其是显著减少Escherichia coli水平及内脏器官Enterobacteriaceae移位。将饮食干预后的SIRT6 KO小鼠菌群再次移植给KO小鼠,依旧能够有效降低KO小鼠组织器官中炎症因子和衰老标志物的表达水平。
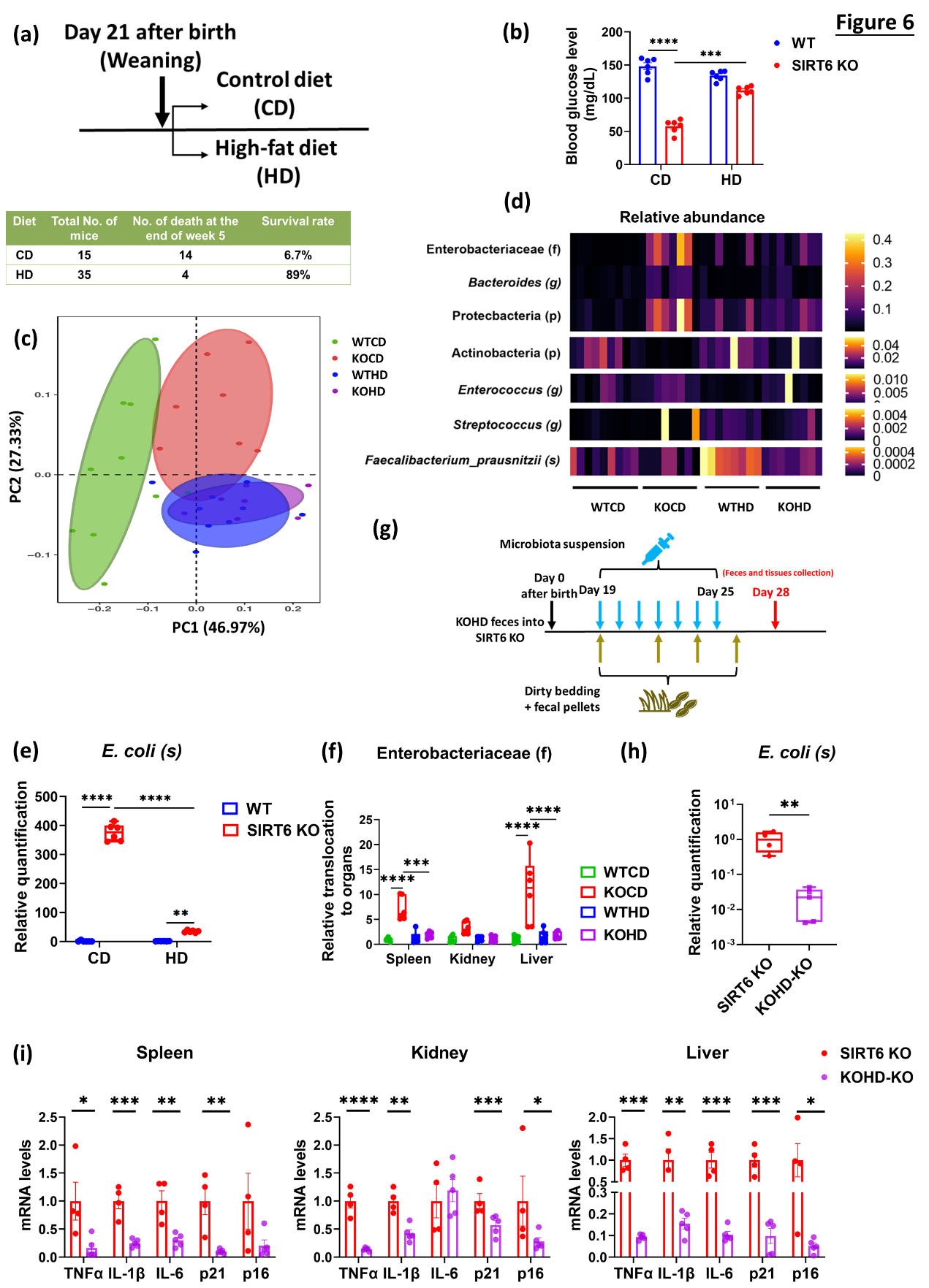
高脂饮食显著降低肠道内Escherichia coli丰度及内脏器官Enterobacteriaceae移位
综上所述,本研究系统地阐述了菌群失调在SIRT6敲除小鼠衰老过程中的重要促进作用,以及高脂饮食能够通过重塑肠道菌群进而减缓SIRT6敲除小鼠早衰。该研究成果进一步强调了基于菌群改善的膳食方案有望成为预防衰老或治疗衰老相关疾病的潜在手段。
以上研究成果于近日在《衰老细胞》(Aging Cell)期刊在线发表了题为“高脂饮食通过改善肠道菌群以降低肠杆菌科移位进而挽救小鼠早衰表型”(Decreased Enterobacteriaceae translocation due to gut microbiota remodeling mediates the alleviation of premature aging by a high-fat diet)的研究论文。
十大老牌网堵网址药我司王钊教授和威尔·康奈尔(Weill Cornell)医我司李忠持博士为本文通讯作者。药我司2021届博士毕业生徐康博士、2019级博士研究生郭彦南与2020级博士研究生王译达为文章共同第一作者。药我司刘清飞副教授,医我司裘莹副教授、高级工程师李雪博士为本课题提供了重要帮助。本研究得到国家自然科学基金、国家重点研发计划、国际科技合作重点项目的支持。
论文链接:
https://doi.org/10.1111/acel.13760
供稿:药我司
编辑:李华山
审核:郭玲